 ЗФТШ
ЗФТШ
- Обучение
- Поступление в ЗФТШ
- О ЗФТШ
- Учителям
- Лекторий
-
Курсы
- Заочное отделение
- Очное отделение
- Факультативы
4.1. Квазистатические процессы
Всякое изменение в термодинамической системе, связанное с изменением хотя бы одного из её параметров состояния, называется термодинамическим процессом.
Пусть в сосуде с поршнем находится некоторая порция газа. Тогда примером термодинамического процесса может служить процесс, в котором при перемещении поршня происходит изменение объёма $$ V$$ газа в сосуде. При этом каждому значению объёма $$ V$$ в состоянии теплового равновесия будет соответствовать определённое значение давления газа $$ p$$. Следовательно, между объёмом газа и его давлением будет существовать некоторая зависимость $$ p\left(V\right)$$, которую можно представить графически, т. е. построить её график в координатах $$ p,V$$.
Каждое равновесное состояние газа изображается на таком графике соответствующей точкой, а сам график изображает изменение параметров газа, т. е. даёт графическое описание теплового процесса.
Но всякое изменение одного из параметров означает, что система вышла из состояния теплового равновесия и ей уже нельзя приписать в целом ни определённого давления, ни определённой температуры.
Например, при быстром опускании поршня (т. е. при сжатии газа) параметры состояния газа (например, давление, плотность и температура) вблизи поршня изменятся довольно существенно. В то же время вдали от поршня изменение состояния газа произойдёт несколько позже. Поэтому газ в целом имеет разные давления и температуры в различных точках, и такое состояние газа нельзя изобразить графически. Возникает естественный вопрос: каким же образом необходимо изменять параметры системы, чтобы можно было в процессе их изменения характеризовать газ тем же числом параметров и использовать уравнение состояния, справедливое, строго говоря, только для состояния теплового равновесия?
Как показывает опыт, любая система, выведенная из состояния равновесия и предоставленная самой себе, переходит по прошествии некоторого времени в состояние теплового равновесия. Процесс перехода к равновесному состоянию называется релаксацией, а время, необходимое для этого, временем релаксации. Это время и определяет скорость изменения параметров системы. Если время перехода из одного равновесного состояния в другое много больше времени релаксации, то все отклонения от равновесного состояния будут успевать исчезать и система будет проходить через ряд равновесных состояний, переходящих одно в другое. Такие процессы называются квазистатическими, потому что при этом в каждый данный момент состояние системы мало отличается от равновесного.
Таким образом, если в рассматриваемом нами примере процесс изменения объёма идёт достаточно медленно, то давление и температура газа во всем объёме успевают сравняться и принимают в каждый момент времени одинаковые по всему объёму значения. Это означает, что в таком процессе газ проходит через последовательность равновесных (почти равновесных) состояний. Так как в равновесном процессе давление $$ p$$, температура $$ T$$ и объём $$ V$$ в каждый момент времени имеют вполне определённые значения, то существуют зависимости между $$ p$$ и $$ T$$, $$ V$$ и $$ T$$, $$ p$$ и $$ V$$. Следовательно, квазистатические процессы можно изображать в виде графиков этих зависимостей, например, $$ p\left(V\right)$$ или $$ V\left(T\right)$$. Неравновесный процесс невозможно изобразить графически.
Ясно, что с помощью уравнения состояния можно изучать только квазистатические процессы. Времена релаксаций, определяющие степень медленности квазистатического процесса, для разных систем и различных тепловых процессов сильно отличаются друг от друга, и для их определения нужно проводить очень трудный и сложный дополнительный анализ. В дальнейшем рассматриваются только квазистатические процессы.
Процессы, протекающие при постоянной массе газа и неизменном значении одного из параметров состояния газа (давление, объём или температура), принято называть изопроцессами. Например, процесс, происходящий при постоянной температуре, называется изотермическим, при постоянном объёме – изохорическим (или изохорным), при постоянном давлении – изобарическим (или изобарным).
4.2. Изотермический процесс. Закон Бойля – Мариотта
В XVII веке независимо друг от друга английский физик Бойль и французский физик Мариотт экспериментально установили закон изменения объёма газа при изменении давления: для данной массы любого газа при постоянной температуре его объём обратно пропорционален давлению.
Закон носит название закона Бойля – Мариотта и обычно записывается в виде:
$$ pV=\mathrm{const}$$,
где значение константы определяется температурой, при которой происходит данный процесс.
График этого процесса (изотерма) в координатах $$ p$$ и $$ V$$ изобразится кривой, определяемой уравнением:
$$ p={\displaystyle \frac{\mathrm{const}}{V}}$$.
Эта кривая, как известно из математики, называется гиперболой. На рисунке $$ 1$$ изображены изотермы одной и той массы газа для двух разных температур $$ {T}_{1}$$ и $$ {T}_{2}$$ $$ ({T}_{2}>{T}_{1})$$. Изотерма, соответствующая бóльшей температуре, проходит выше, так как при одинаковых объёмах бóльшей температуре соответствует и бóльшее давление.
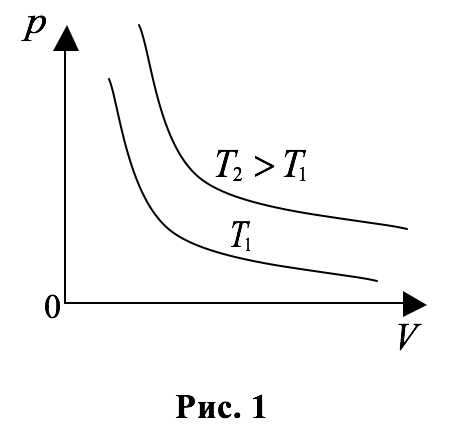 |
4.3. Изобарический процесс. Закон Гей-Люссака
Поместим газ в сосуд с вертикальными стенками и подвижным поршнем, имеющим массу $$ {m}_{\mathrm{п}}g$$ и площадь сечения $$ S$$ который может перемещаться без трения (рис. $$ 2$$). Пусть на поршень сверху действует атмосферное давление $$ {p}_{0}$$. Рассмотрим равновесное состояние газа, характеризуемое давлением $$ p$$. Величину этого давления найдём из условия механического равновесия для поршня.
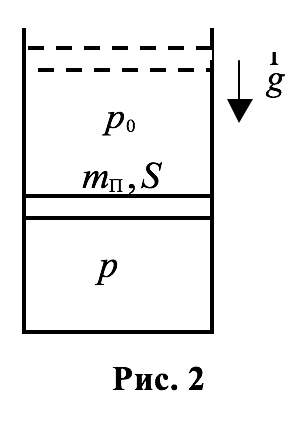 |
На поршень действуют две силы, направленные вертикально вниз (сила тяжести $$ {m}_{\mathrm{п}}$$ и сила давления атмосферы $$ {p}_{0}S$$), и направленная вертикально вверх сила давления со стороны газа под поршнем, значение которой равно $$ pS$$. Условие равновесия поршня $$ -$$ равенство нулю равнодействующей этих сил. Отсюда для давления $$ p$$ газа находим:
$$ p={p}_{0}+{\displaystyle \frac{{m}_{\mathrm{п}}g}{S}}$$
Внешнее давление на газ также равно $$ p$$. Как показывает опыт, при квазистатическом (медленном) нагревании газа под поршнем при постоянном внешнем давлении, объём всех без исключения газов увеличивается, а при охлаждении уменьшается.
Исследуя на опыте тепловое расширение газов при постоянном давлении, французский учёный Гей-Люссак открыл, что объём $$ V$$ газа данной массы при изменении температуры $$ t\left({}^{\circ }\mathrm{C}\right)$$ изменяется по линейному закону:
$$ V={V}_{0}(1+\alpha t)$$.
Здесь $$ {V}_{0} -$$ объём газа при температуре $$ 0{}^{\circ }\mathrm{C}$$, $$ \alpha -$$ коэффициент объёмного расширения при постоянном давлении. Оказалось, что для всех газов $$ \alpha $$ принимает одно и то же значение, равное $$ 1/273{}^{\circ }\mathrm{C}$$.
4.4. Изохорический процесс. Закон Шарля
Рассмотрим теперь процесс нагревания газа при постоянном объёме, или, как говорят, процесс изохорического нагревания газа. Поместим для этого газ в герметический сосуд, например, в металлический котёл с плотно завинчивающейся крышкой. Будем нагревать газ в котле, измеряя его температуру и давление. Как показывает опыт, давление газа внутри котла увеличивается с ростом температуры.
Зависимость давления газа от температуры при неизменном объёме была экспериментально установлена французским физиком Шарлем. Согласно закону Шарля, давление $$ p$$ газа данной массы при изменении температуры $$ t\left({}^{\circ }\mathrm{C}\right)$$ изменяется по линейному закону:
$$ p={p}_{0}(1+\gamma t)$$.
Здесь $$ {p}_{0} -$$ давление газа при температуре $$ 0{}^{\circ }\mathrm{C}$$, $$ \gamma -$$ термический коэффициент давления. Оказалось, что для всех газов $$ \gamma $$ принимает одно и то же значение, равное $$ 1/273{}^{\circ }\mathrm{C}$$. Заметим, что коэффициент $$ \gamma $$ равен коэффициенту $$ \alpha $$ в законе Гей-Люссака.
4.5. Абсолютная шкала температур
Законы Гей-Люссака и Шарля выглядят гораздо проще, если вместо температурной шкалы Цельсия $$ t\left({}^{\circ }\mathrm{C}\right)$$ ввести шкалу, предложенную английским физиком Кельвином. Связь между температурой $$ T$$ по шкале Кельвина и температурой $$ t$$ по шкале Цельсия даётся формулой:
$$ T=t+{\displaystyle \frac{1}{\alpha }}=t+\frac{1}\gamma =t+273$$.
Шкалу Кельвина называют абсолютной шкалой температур. На новой температурной шкале нулю градусов Цельсия соответствует температура $$ {T}_{0}=273$$ градуса (точнее, $$ \mathrm{273,15}$$). Единица измерения температуры называется кельвином и обозначается буквой $$ \mathrm{К}$$. Изменению температуры на $$ 1$$ градус Цельсия соответствует её изменению на $$ 1$$ кельвин. Комнатной температуре $$ t=20{}^{\circ }\mathrm{C}$$ по шкале Цельсия соответствует температура $$ T=293 \mathrm{К}$$ по шкале Кельвина.
Законы Гей-Люссака и Шарля при этом примут вид:
$$ V={V}_{0}\alpha ·\left({\displaystyle \frac{1}{\alpha }}+t\right)=\alpha {V}_{0}T$$ (закон Гей-Люссака),
$$ p={p}_{0}\gamma \left({\displaystyle \frac{1}{\gamma }}+t\right)=\gamma {p}_{0}T$$ (закон Шарля),
где $$ {V}_{0}$$ и $$ {p}_{0} -$$ объём и давление газа при температуре $$ {T}_{0}$$.
Как видно из уравнения для закона Гей-Люссака, график изобарического процесса (изобара) в координатах $$ V$$ и $$ T$$ представляет собой отрезок, лежащий на прямой линии, проходящей через начало координат. На рисунке 3 показаны две изобары при различных давлениях $$ {p}_{1}$$ и $$ {p}_{2} ({p}_{2}>{p}_{1})$$. Давление, при котором проходит процесс, можно изменять, используя поршни разной массы. Вторая изобара проходит ниже первой, так как при одной и той же температуре бóльшему давлению соответствует меньший объём.
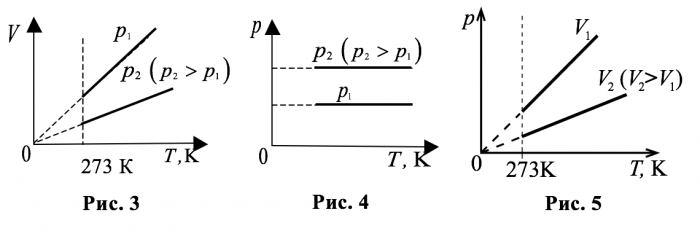 |
В координатах $$ p$$ и $$ T$$ графики изобарических процессов представляют собой прямые линии, параллельные оси $$ T$$ (рис. 4).
График изохорического процесса (изохора, закон Шарля) в координатах $$ p$$ и $$ T$$ представляет собой отрезок, лежащий на прямой линии, проходящей через начало координат. На рисунке 5 показаны две изохоры при различных объёмах $$ {V}_{1}$$ и $$ {V}_{2} ({V}_{2}>{V}_{1})$$. Вторая изохора проходит ниже первой, так как при одной и той же температуре бóльшему давлению соответствует меньший объём.